 par Véto-pharma
par Véto-pharma En 2014, Véto-pharma a inauguré son rucher expérimental. Celui-ci est devenu un pilier majeur de sa recherche et développement. Associé à un laboratoire R&D ad hoc mis en œuvre l’année suivante, le rucher a considérablement renforcé les capacités de Véto-pharma dans la lutte contre le varroa.
En 2018, l’équipe innovation composée d’ingénieurs, de chercheurs et de techniciens apicoles a intensifié ses efforts en recherche contre le varroa en développant ses propres méthodes de screening de molécules. Entre la phase de tests de nouveaux actifs et la mise sur le marché d’un nouveau médicament les délais varient. Aussi, Véto-pharma œuvre avec détermination pour accélérer dans la mesure du possible le processus. Plus d’une centaine d’actifs ont été évalués afin d’identifier les futurs médicaments efficaces contre le varroa, sûrs pour les colonies, les utilisateurs et les consommateurs.
Beaucoup se questionnent : A quand un nouveau produit disponible sur le marché ? La réponse est complexe, car de nombreux paramètres et obligations réglementaires sont à prendre en compte. La transition de la découverte de l’efficacité d’un actif à la commercialisation d’un médicament est un processus long qui prendre de nombreuses années. Une des principales difficultés réside dans la toxicité des molécules. Bien que certaines soient efficaces contre le varroa, elles peuvent être très toxiques pour les abeilles. Par exemple, de nombreuses huiles essentielles, malgré leur efficacité, s’avèrent dangereuses pour les abeilles à des doses optimales. En outre, obtenir suffisamment de varroas vivants pour les tests est aussi un autre défi majeur. Le rucher expérimental joue alors un rôle crucial en fournissant les ressources nécessaires aux essais en laboratoire.

Le projet de screening continuera jusqu’à ce qu’un ou plusieurs actifs soient entièrement validés pour leur efficacité contre le varroa et leur innocuité envers les abeilles. Actuellement, ces validations se font principalement in vitro ou en cagette pour les abeilles. Une fois un actif identifié à l’étape de screening, il entre en développement préclinique pour définir son activité pharmacologique, pharmacocinétique et toxicologique. Ensuite, il passe en développement clinique, où une formulation finale est choisie et testée lors d’essais cliniques. Ce n’est qu’après la validation clinique et la constitution d’un dossier d’Autorisation de Mise sur le Marché (AMM) que le processus d’enregistrement peut commencer. L’ensemble de ces étapes prend en moyenne 5 à 10 ans avant d’aboutir à un médicament utilisable par les apiculteurs.
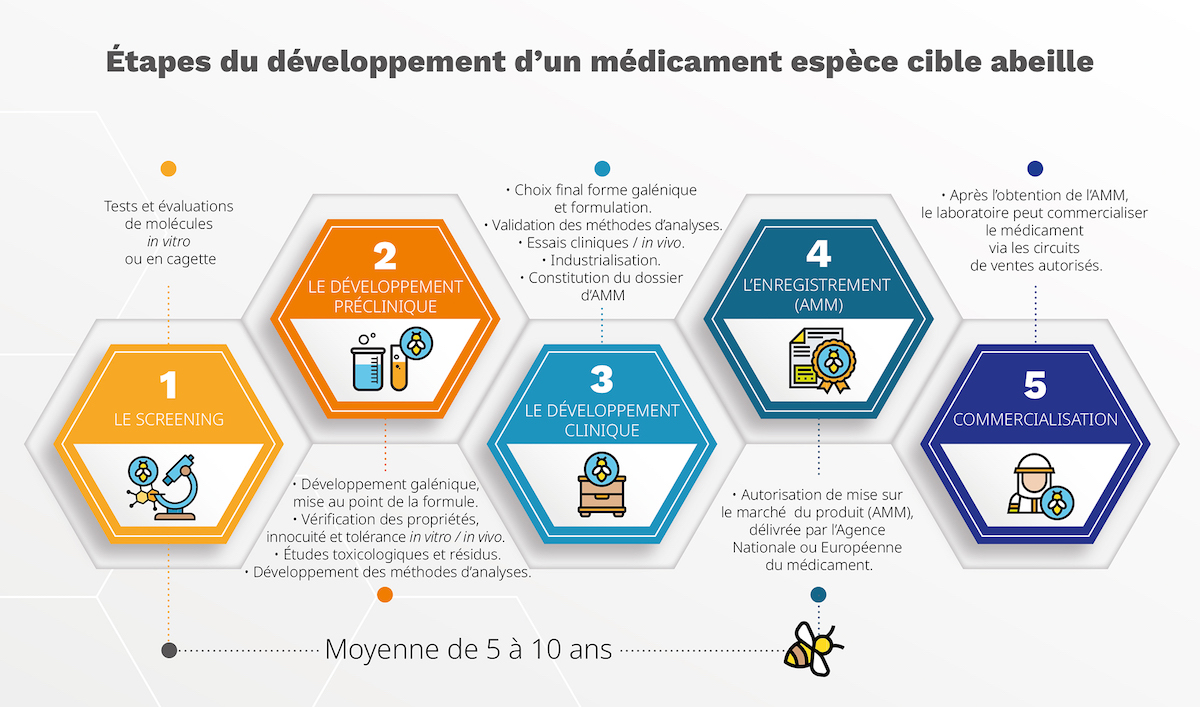
Les molécules sont soumises à une série de tests pour évaluer leurs propriétés chimiques et pharmacologiques. Cette étape permet d’identifier celles ayant un potentiel thérapeutique. Véto-pharma a développé une méthode spécifique pour évaluer les molécules efficaces et peu toxiques pour les abeilles.

Cette phase comprend le développement galénique et analytique, où la formulation du produit est mise au point, c’est-à-dire la “recette” du médicament. La substance active est incorporée dans une forme galénique (solution, pâte, gel, poudre…) pour vérifier ses propriétés pharmacologiques chez l’animal cible, ici l’abeille, ainsi que son innocuité et sa tolérance. Des études de toxicologie et de résidus sont également réalisées.

Une fois la forme galénique et la formulation finale choisies, les essais cliniques commencent. Ils visent à confirmer les propriétés du médicament dans des conditions normales d’utilisation et sur le “terrain”, et à démontrer son effet thérapeutique dans le “monde réel”. Toutes les études réalisées sont compilées et réunies dans un dossier de demande d’autorisation de mise sur le marché (AMM) qui sera transmis aux autorités pour évaluation.

Avant d’être commercialisés, les médicaments vétérinaires, dont la fabrication a été industrialisée, doivent obtenir une Autorisation de Mise sur le Marché (AMM) délivrée par l’Agence nationale du médicament vétérinaire (Anses-ANMV) ou l’Agence européenne du médicament (EMA). L’EMA délivre des AMM dites centralisées valables dans l’Union européenne dont la France.
Quelle que soit la procédure, l’AMM est accordée sur la base d’exigences similaires. Elles conduisent à une évaluation du rapport bénéfices / risques.
Le processus de développement d’un médicament vétérinaire est donc long et complexe. Véto-pharma reste déterminé plus que jamais à investir annuellement entre 8 et 10 % de ses ressources en innovation, avec une équipe dédiée d’une dizaine de personnes. En plus des projets internes, Véto-pharma collabore avec des partenaires externes, comme l’Université Simon Fraser au Canada, pour optimiser la recherche de traitements contre le varroa, que ce soient pour des nouveaux actifs ou des nouvelles technologies galéniques. L’objectif principal est de répondre aux besoins des apiculteurs de demain.
 par Véto-pharma
par Véto-pharma  par Véto-pharma
par Véto-pharma  par Véto-pharma
par Véto-pharma Rejoignez la communauté Véto-pharma et recevez notre newsletter trimestrielle ainsi que nos actualités apicoles ponctuelles. Vous pourrez vous en désabonner à tout moment si nos contenus ne vous conviennent pas, et vos données ne seront jamais cédées à un tiers !
© 2019-2025, Véto-pharma. Tous droits réservés